[대전=이데일리 박진환 기자] 브이픽스메디칼은 지난 21일 미국 식품의약국(FDA)으로부터 ‘cCeLL-In vivo’에 대한 510(k) 승인을 획득했다고 28일 밝혔다. cCeLL-In vivo는 초소형 공초점 현미경 기술 기반으로 신경외과 의사가 손으로 잡고 환자의 장기에 기기를 접촉해 침습적 생검 없이 세포 수준의 디지털 영상을 실시간으로 획득하는 의료기기이다. 이 시스템은 인도시아닌 그린(ICG) 염료를 활용해 고해상도 형광 현미경 영상을 제공할 수 있고, 수술 중 실시간으로 뇌종양 및 뇌혈관과 미세구조를 시각화하는데 도움을 줘 근치적 종양 절제와 정상 뇌 조직 보호에 크게 기여할 수 있다.
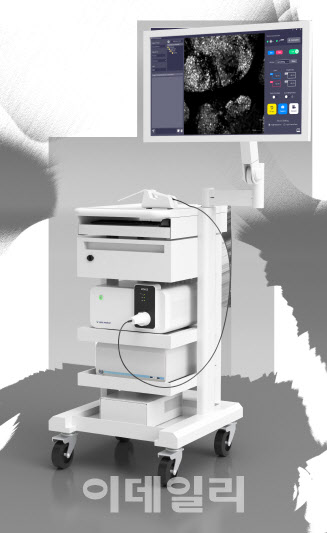 | | 브이픽스메디칼의 cCeLL-In vivo 제품. (사진=브이픽스메디칼 제공) |
|
브이픽스메디칼은 글로벌 경쟁력이 있는 초소형 공초점 현미경 기술을 보유하고 있는 기업이다.산업은행, 산업은행캐피탈, 쿼드자산운용 등으로부터 기술력을 인정 받아 투자 및 지원을 받아 국내 최초로 암 수술용 초소형 형광 현미경을 개발했다. ICG 형광 이미징 현미경 기술로 미국 FDA 인증을 받은 사례는 전 세계에서 2번째이다. 특히 신경외과 수술에 실시간으로 사용할 수 있는 ICG 형광 현미경은 FDA 인증 전례가 없어 국산 의료기기가 업계 표준으로 자리 잡을 것으로 기대된다.
브이픽스메디칼의 황경민 대표는 “이번 FDA 승인을 통해 신경외과 의사들에게 실시간으로 수술 중 결정을 내릴 수 있는 강력한 도구를 제공할 수 있게 됐다”며 “cCeLL - In vivo의 FDA 승인은 우리의 제품의 안전성과 유효성을 의료기기 최대 시장인 미국에서 인정받았다는데 큰 의미가 있다. 향후 뇌종양 분야를 넘어 다양한 암 종에 적용할 수 있는 제품으로 확대할 것”이라고 말했다.
브이픽스메디칼은 올해부터 고려대안암병원, 서울대병원, 삼성서울병원, 보라매병원에서 뇌종양 수술 환자 대상 임상 연구를 시작했다. 이번 FDA 승인을 통해 국제 다기관 임상으로 확대해 실 사례를 통한 글로벌 시장 진출을 본격화한다는 구상이다.